Strukturformeln, Steroide und der programmierte Alterungsprozess
Wenn Sie die vorangegangenen Konzepte einem Mainstream-Wissenschaftler vorlegen, werden Sie aller Wahrscheinlichkeit nach auf große Skepsis stoßen. Das liegt daran, dass der herkömmlichen Denkweise zufolge jedes Hormon in einen bestimmten Rezeptor passt und keine andere Funktion hat als ein Schlüssel, der ein Schloss öffnet. Meiner Ansicht nach ist dies bei vielen Hormonen und Substanzen aber nur die halbe Wahrheit.
Nehmen wir beispielsweise Vitamin D3: Es gibt Vitamin-D3-Rezeptoren, an die das Vitamin bindet – und wo der Vitamin-Rezeptor-Komplex dann an die DNS bindet, um diverse Gene zu steuern.
Ich glaube jedoch, dass es mehrere Hormone gibt (vor allem Steroide), bei denen man feststellen wird, dass sie sich direkt und ohne die Notwendigkeit eines Rezeptors mit der DNS verbinden. Man könnte das als sekundäre Funktion bezeichnen, die nach und nach den Alterungsprozess beeinflusst, indem sie den Methylierungsgrad der DNS steuert. Es gibt auch etliche Arzneistoffe, die ohne Rezeptoren funktionieren und direkt an die DNS binden – also ist diese Idee gar nicht so spekulativ.
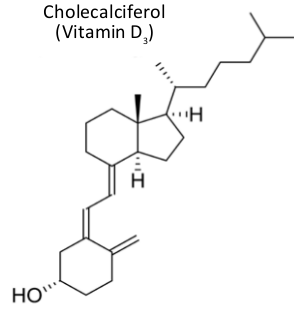
In meinem ersten veröffentlichten wissenschaftlichen Aufsatz aus dem Jahr 1998 stellte ich die Hypothese auf, dass die „guten“ Hormone mit der Methylierung der DNS zu tun haben. Ich nahm an, dass sie auf irgendeine Weise mit dem Transfer von Methylgruppen an die DNS zusammenhängen und dieser Transfer von Antioxidantien katalysiert wird. Damals wusste ich noch nicht, dass Steroidhormone genau dieselbe chemische Strukturformel haben wie DNS-Basenpaare; beide weisen an ihren Außenseiten Antioxidantien und Methylgruppen auf. Ursprünglich vermutete ich, dass drei unterschiedliche Substanzen in der Nähe der DNS zusammenkommen müssen. Die obige Analyse macht jedoch deutlich, dass diese drei Substanzen häufig schon in einer einzigen Verbindung vorkommen.
Es gibt noch ein paar andere lebensverlängernde Substanzen, die ich nicht so leicht einer Kategorie zuordnen kann, weil sie ziemlich groß sind und anscheinend ihren eigenen Regeln folgen. Nehmen wir zum Beispiel das Immunsuppressivum Rapamycin (Sirolimus), das in Studien die durchschnittliche und maximale Lebensdauer von Mäusen verlängert hat:
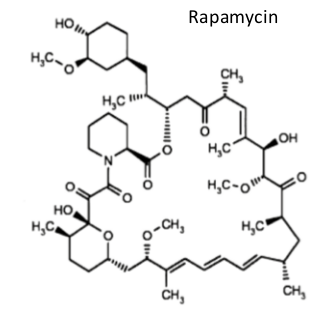
Möglicherweise nimmt Rapamycin nach seinem Abbau im Körper eine Steroidform an. Jedenfalls ist es mit einer Menge Antioxidantien und Methylgruppen ausgestattet. Vielleicht folgt es also ebenfalls den obigen Regeln.
Was haben die Hormone, deren Spiegel im Alter ansteigt und die uns altern lassen, nun gemeinsam? Zum jetzigen Zeitpunkt kann ich nur sagen, dass „schlechte“ Hormone tendenziell recht groß sind. Ich bin schon längere Zeit der Meinung, dass die Größe eines Hormons mit seinem evolutionären Alter zu tun hat – je größer, desto älter. Schließlich musste sich bei jeder Vergrößerung des Hormons auch ein größerer Rezeptor entwickeln.
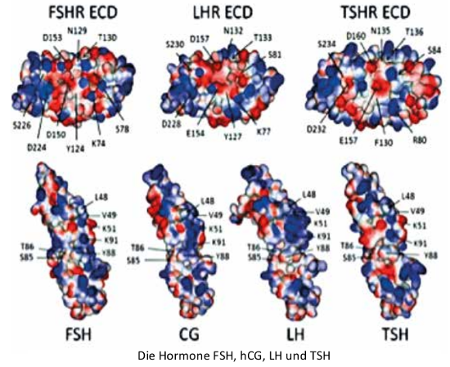
Ich konnte über TSH aber nur herausfinden, dass der Prozentsatz der Bevölkerung mit einem erhöhten TSH-Spiegel im Alter von 19 bis 80 Jahren von 2 auf 14 Prozent ansteigt. Andererseits gibt es aber auch eine Bevölkerungsgruppe, in der der TSH-Spiegel mit zunehmendem Alter sinkt. Vielleicht ist TSH also ein großes Hormon, das sich nicht unbedingt schlecht auswirken muss.
Es gibt noch viele Rätsel zu lösen – aber bald wird auch die Mainstream-Wissenschaft erkennen, dass es ein genetisches Alterungsprogramm gibt. Und dann können wir darangehen, das Problem des Alterns gemeinsam zu lösen.


 Jeff Bowles ist für sein Selbstexperiment mit hochdosiertem Vitamin D3, seinen lockeren Schreibstil und dafür bekannt, notorisch originell zu denken. In diesem bearbeiteten Auszug aus seinem neuen Buch schildert er, was er über die chemische Struktur von Substanzen herausgefunden hat, die als gesund gelten und den Alterungsprozess verlangsamen können.
Jeff Bowles ist für sein Selbstexperiment mit hochdosiertem Vitamin D3, seinen lockeren Schreibstil und dafür bekannt, notorisch originell zu denken. In diesem bearbeiteten Auszug aus seinem neuen Buch schildert er, was er über die chemische Struktur von Substanzen herausgefunden hat, die als gesund gelten und den Alterungsprozess verlangsamen können.
Kommentare
01. September 2019, 11:30 Uhr, permalink
Lotus8568
Lieber Mr. Bowles, vielen Dank für diese Lehreiche Ausführung!!!
Habe heute was über Propolis gelesen und sieh da auch CH3...
Viele liebe Grüße aus Deutschland
Kommentar schreiben